Proučevanje procesov, ki se dogajajo v statističnih sistemih, je zapleteno zaradi minimalne velikosti delcev in njihovega ogromnega števila. Vsak delec je praktično nemogoče obravnavati posebej, zato se uvedejo statistične količine: povprečna hitrost delcev, njihova koncentracija, masa delcev. Formula, ki označuje stanje sistema ob upoštevanju mikroskopskih parametrov, se imenuje osnovna enačba molekularno-kinetične teorije plinov (MKT).
Malo o povprečni hitrosti delcev
Določanje hitrosti delcev je bilo najprej izvedeno eksperimentalno. Znan eksperiment iz šolskega učnega načrta, ki ga je izvedel Otto Stern, je omogočil ustvarjanje ideje o hitrostih delcev. Med poskusom so preučevali gibanje atomov srebra v vrtečih se valjih: najprej v stacionarnem stanju naprave, nato pa pri vrtenju z določeno kotno hitrostjo.
Kot rezultat, je bilo ugotovljeno, da hitrost srebrovih molekul presega hitrost zvoka in je 500 m/s. Dejstvo je precej zanimivo, saj človek težko občuti takšne hitrosti gibanja delcev v snoveh.
Idealni plin
Nadaljujte z raziskavoZdi se, da je to mogoče le v sistemu, katerega parametre je mogoče določiti z neposrednimi meritvami s fizičnimi instrumenti. Hitrost se meri z merilnikom hitrosti, vendar je ideja, da bi merilnik hitrosti pritrdili na en delček, absurdna. Neposredno je mogoče izmeriti samo makroskopski parameter, povezan z gibanjem delcev.
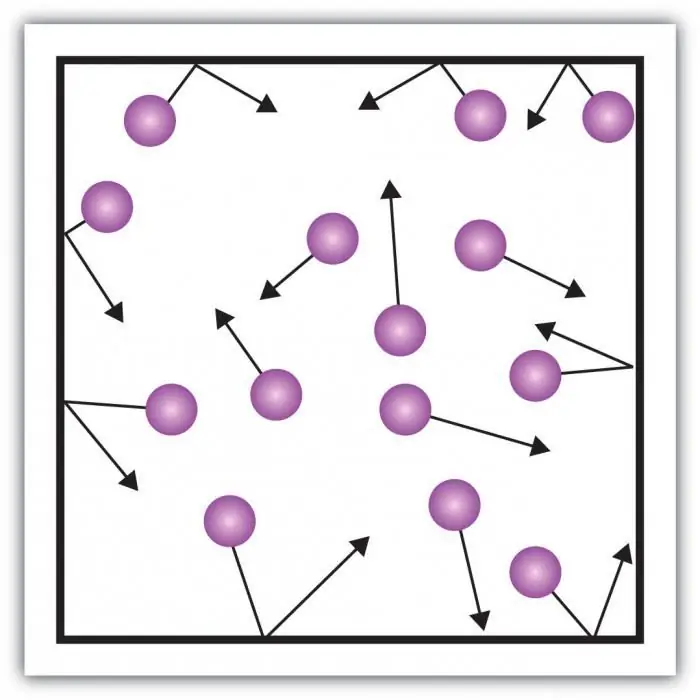
Upoštevajte tlak plina. Pritisk na stene posode nastane zaradi udarcev molekul plina v posodi. Posebnost plinastega stanja snovi je v dovolj velikih razdaljah med delci in njihovi majhni medsebojni interakciji. To vam omogoča neposredno merjenje njegovega tlaka.
Za vsak sistem medsebojno delujočih teles je značilna potencialna energija in kinetična energija gibanja. Pravi plin je zapleten sistem. Spremenljivost potencialne energije ni primerna za sistematizacijo. Težavo je mogoče rešiti z uvedbo modela, ki nosi značilne lastnosti plina, s čimer se odpravi zapletenost interakcije.
Idealni plin je stanje snovi, pri katerem je interakcija delcev zanemarljiva, potencialna energija interakcije teži k nič. Za pomembno lahko štejemo samo energijo gibanja, ki je odvisna od hitrosti delcev.
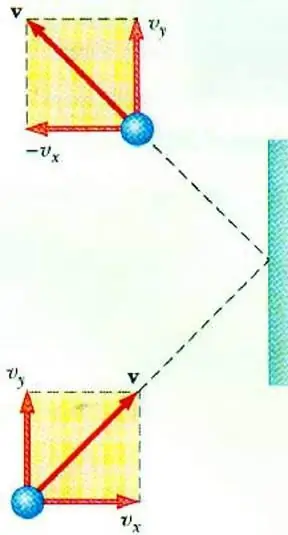
Idealni tlak plina
Razkrivanje razmerja med tlakom plina in hitrostjo njegovih delcev omogoča osnovno enačbo MKT idealnega plina. Delec, ki se giblje v posodi, ob udarcu v steno nanjo prenese impulz, katerega vrednost lahko določimo na podlagi drugega zakonaNewton:
F∆t=2m0vx
Sprememba gibalne količine delca med elastičnim udarcem je povezana s spremembo vodoravne komponente njegove hitrosti. F je sila, ki deluje s strani delca na steno za kratek čas t; m0 - masa delcev.
Vsi plinski delci trčijo s površino območja S v času ∆t, se gibljejo v smeri površine s hitrostjo vx in se nahajajo v jeklenki prostornine Sυ x Δt. Pri koncentraciji delcev n se natanko polovica molekul premakne proti steni, druga polovica pa v nasprotni smeri.
Po upoštevanju trka vseh delcev lahko zapišemo Newtonov zakon za silo, ki deluje na območje:
F∆t=nm0vx2S∆t
Ker je tlak plina opredeljen kot razmerje sile, ki deluje pravokotno na površino, do površine slednje, lahko zapišemo:
p=F: S=nm0vx2
Nastala relacija kot osnovna enačba MKT ne more opisati celotnega sistema, saj se upošteva samo ena smer gibanja.
Maxwellova distribucija
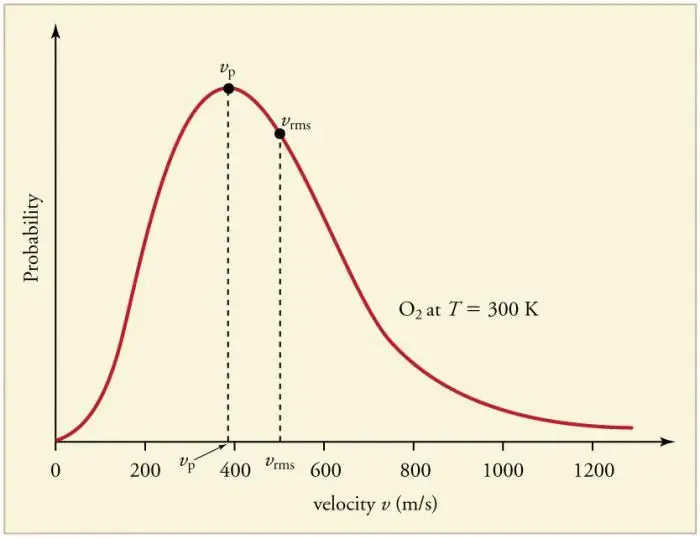
Nenehni pogosti trki plinskih delcev s stenami in med seboj vodijo k vzpostavitvi določene statistične porazdelitve delcev glede na hitrosti (energije). Smeri vseh vektorjev hitrosti se izkažejo za enako verjetne. Ta porazdelitev se imenuje Maxwellova distribucija. Leta 1860 je bil ta vzorecki ga je na podlagi MKT izpeljal J. Maxwell. Glavni parametri zakona o porazdelitvi se imenujejo hitrosti: verjetna, ki ustreza največji vrednosti krivulje, in povprečni korenski vkv=√‹v2 › - srednji kvadrat hitrosti delcev.
Povišanje temperature plina ustreza povečanju hitrosti.
Na podlagi dejstva, da so vse hitrosti enake in imajo njihovi moduli enako vrednost, lahko domnevamo:
‹v2›=‹vx2› + ‹v y2› + ‹vz2›, od: ‹ vx2›=‹v2›: 3
Osnovna enačba MKT ob upoštevanju povprečne vrednosti tlaka plina je:
p=nm0‹v2›: 3.
Ta odnos je edinstven po tem, da določa razmerje med mikroskopskimi parametri: hitrostjo, maso delcev, koncentracijo delcev in tlakom plina na splošno.
Z uporabo koncepta kinetične energije delcev lahko osnovno enačbo MKT prepišemo drugače:
p=2nm0‹v2›: 6=2n‹Ek›: 3
Tlak plina je sorazmeren povprečni vrednosti kinetične energije njegovih delcev.
temperatura
Zanimivo je, da je za konstantno količino plina v zaprti posodi mogoče povezati tlak plina in povprečno vrednost energije gibanja delcev. V tem primeru je mogoče tlak izmeriti z merjenjem energijedelci.
Kaj storiti? Kakšno vrednost lahko primerjamo s kinetično energijo? Temperatura se izkaže za takšno vrednost.

Temperatura je merilo toplotnega stanja snovi. Za merjenje se uporablja termometer, katerega osnova je toplotna ekspanzija delovne tekočine (alkohol, živo srebro) pri segrevanju. Lestvica termometra je narejena eksperimentalno. Običajno so na njem postavljene oznake, ki ustrezajo položaju delovne tekočine med fizikalnim procesom, ki poteka pri konstantnem toplotnem stanju (vrela voda, taljenje ledu). Različni termometri imajo različne lestvice. Na primer, Celzij, Fahrenheit.

Univerzalna temperaturna lestvica
Plinski termometri se lahko štejejo za bolj zanimive v smislu neodvisnosti od lastnosti delovne tekočine. Njihov obseg ni odvisen od vrste uporabljenega plina. V takšni napravi lahko hipotetično izpostavimo temperaturo, pri kateri se tlak plina nagiba k nič. Izračuni kažejo, da ta vrednost ustreza -273,15 oC. Temperaturna lestvica (absolutna temperaturna lestvica ali Kelvinova lestvica) je bila uvedena leta 1848. Za glavno točko te lestvice je bila vzeta možna temperatura ničelnega tlaka plina. Odsek enote lestvice je enak vrednosti enote Celzijeve lestvice. Zdi se, da je pri proučevanju plinskih procesov bolj priročno zapisati osnovno enačbo MKT z uporabo temperature.
Razmerje med tlakom in temperaturo
Empirično lahko to preveritesorazmernost tlaka plina z njegovo temperaturo. Hkrati je bilo ugotovljeno, da je tlak neposredno sorazmeren s koncentracijo delcev:
P=nkT,
kjer je T absolutna temperatura, k je konstanta enaka 1,38•10-23J/K.
Osnovna vrednost, ki ima konstantno vrednost za vse pline, se imenuje Boltzmannova konstanta.
Če primerjamo odvisnost tlaka od temperature in osnovno enačbo plinov MKT, lahko zapišemo:
‹Ek›=3kT: 2
Povprečna vrednost kinetične energije gibanja molekul plina je sorazmerna z njeno temperaturo. To pomeni, da lahko temperatura služi kot merilo kinetične energije gibanja delcev.






