Pri proučevanju obnašanja plinov v fiziki veliko pozornosti namenjamo izoprocesom, torej takšnim prehodom med stanji sistema, pri katerih se ohrani en termodinamični parameter. Vendar pa obstaja plinski prehod med stanji, ki ni izoproces, ima pa pomembno vlogo v naravi in tehnologiji. To je adiabatski proces. V tem članku ga bomo podrobneje obravnavali, pri čemer se bomo osredotočili na to, kaj je plinsko adiabatni eksponent.
adiabatski proces
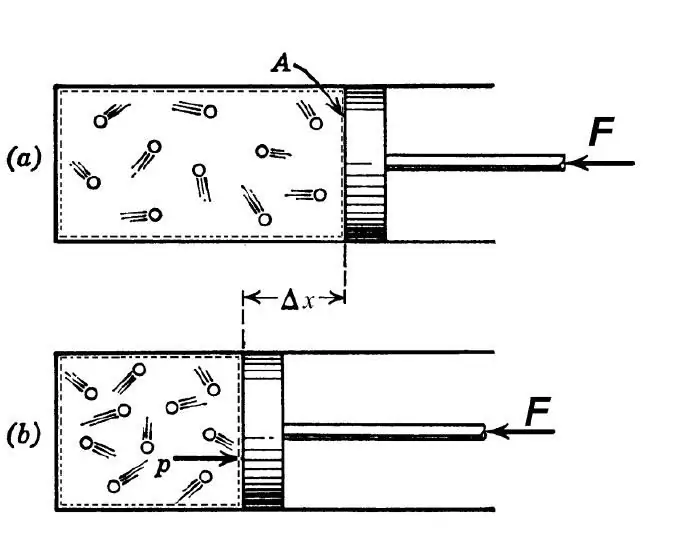
Po termodinamični definiciji se adiabatski proces razume kot tak prehod med začetnim in končnim stanjem sistema, zaradi katerega ni izmenjave toplote med zunanjim okoljem in preučevanim sistemom. Tak postopek je možen pod naslednjima dvema pogojema:
- toplotna prevodnost med zunanjim okoljem insistem je nizek iz enega ali drugega razloga;
- hitrost postopka je visoka, zato izmenjava toplote nima časa za izvedbo.
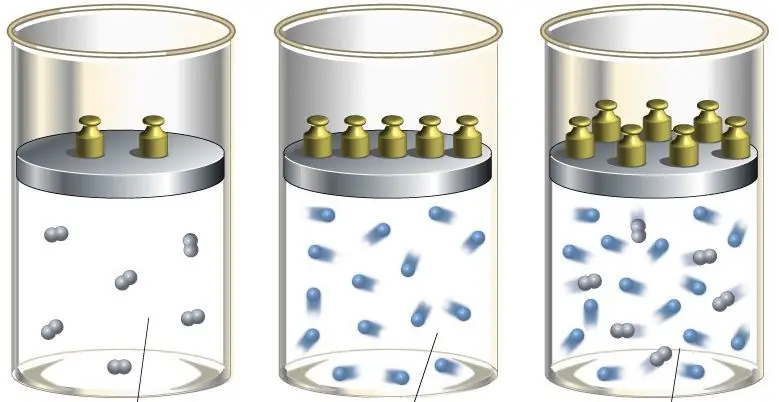
V inženirstvu se adiabatni prehod uporablja tako za segrevanje plina med njegovim ostrim stiskanjem kot za hlajenje med hitrim širjenjem. V naravi se zadevni termodinamični prehod kaže, ko se zračna masa dvigne ali spusti po pobočju hriba. Takšni vzponi in padci vodijo do spremembe rosišča v zraku in padavin.
Poissonova enačba za adiabatni idealni plin

Idealni plin je sistem, v katerem se delci naključno gibljejo z velikimi hitrostmi, med seboj ne delujejo in so brez dimenzij. Tak model je zelo preprost v smislu svojega matematičnega opisa.
Po definiciji adiabatskega procesa lahko v skladu s prvim zakonom termodinamike zapišemo naslednji izraz:
dU=-PdV.
Z drugimi besedami, plin, ki se širi ali krči, deluje PdV zaradi ustrezne spremembe njegove notranje energije dU.
V primeru idealnega plina, če uporabimo enačbo stanja (Clapeyron-Mendelejev zakon), lahko dobimo naslednji izraz:
PVγ=konst.
Ta enakost se imenuje Poissonova enačba. Ljudje, ki poznajo fiziko plinov, bodo opazili, da če je vrednost γ enaka 1, bo Poissonova enačba prešla v Boyle-Mariotteov zakon (izotermniproces). Vendar je taka transformacija enačb nemogoča, saj je γ za katero koli vrsto idealnega plina večji od ena. Količina γ (gama) se imenuje adiabatni indeks idealnega plina. Oglejmo si podrobneje njegov fizični pomen.
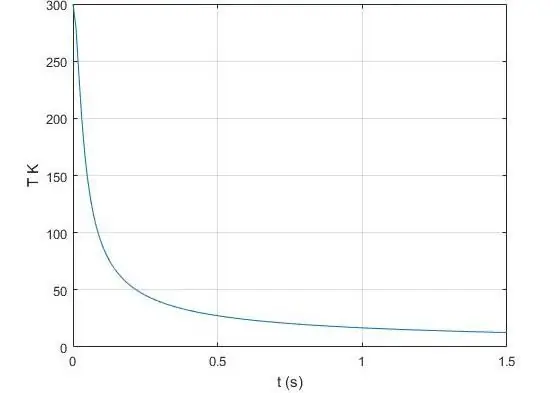
Kakšen je adiabatni eksponent?
Eksponent γ, ki se pojavi v Poissonovi enačbi za idealni plin, je razmerje med toplotno kapaciteto pri konstantnem tlaku in isto vrednostjo, vendar že pri konstantni prostornini. V fiziki je toplotna kapaciteta količina toplote, ki jo je treba prenesti ali odvzeti iz določenega sistema, da lahko spremeni svojo temperaturo za 1 Kelvin. Izobarično toplotno kapaciteto bomo označili s simbolom CP, izohorično toplotno kapaciteto pa s simbolom CV. Potem velja enakost za γ:
γ=CP/CV.
Ker je γ vedno večji od ena, kaže, kolikokrat izobarična toplotna zmogljivost preučevanega plinskega sistema presega podobno izohorično karakteristiko.
Toplotne zmogljivosti CP in CV
Za določitev adiabatnega eksponenta je treba dobro razumeti pomen količin CP in CV. Da bi to naredili, bomo izvedli naslednji miselni poskus: predstavljajte si, da je plin v zaprtem sistemu v posodi s trdnimi stenami. Če se posoda segreje, se vsa prenesena toplota idealno pretvori v notranjo energijo plina. V takšni situaciji bo veljala enakost:
dU=CVdT.
VrednostCVopredeljuje količino toplote, ki jo je treba prenesti v sistem, da se izohorično segreje za 1 K.
Sedaj recimo, da je plin v posodi s premikajočim se batom. V procesu ogrevanja takšnega sistema se bo bat premikal, kar bo zagotovilo, da se vzdržuje stalen tlak. Ker bo entalpija sistema v tem primeru enaka produktu izobarične toplotne kapacitete in spremembe temperature, bo prvi zakon termodinamike imel obliko:
CPdT=CVdT + PdV.
Od tu je razvidno, da je CP>CV, saj je v primeru izobarične spremembe stanj potrebno porabijo toploto ne samo za povečanje temperature sistema in s tem njegove notranje energije, temveč tudi za delo, ki ga opravi plin med njegovo ekspanzijo.
Vrednost γ za idealen enoatomski plin
Najenostavnejši plinski sistem je enoatomski idealni plin. Recimo, da imamo 1 mol takega plina. Spomnimo se, da pri izobaričnem segrevanju 1 mol plina za samo 1 Kelvin deluje enako R. Ta simbol se običajno uporablja za označevanje univerzalne plinske konstante. Enako je 8,314 J / (molK). Če za ta primer uporabimo zadnji izraz v prejšnjem odstavku, dobimo naslednjo enakost:
CP=CV+ R.
Od koder lahko določite vrednost izohorične toplotne kapacitete CV:
γ=CP/CV;
CV=R/(γ-1).
Znano je, da za en molenoatomski plin, je vrednost izohorične toplotne kapacitete:
CV=3/2R.
Iz zadnjih dveh enakosti sledi vrednost adiabatskega eksponenta:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Upoštevajte, da je vrednost γ odvisna izključno od notranjih lastnosti plina samega (od poliatomske narave njegovih molekul) in ni odvisna od količine snovi v sistemu.
Odvisnost γ od števila stopenj svobode
Enčba za izohorično toplotno kapaciteto enoatomskega plina je bila zapisana zgoraj. Koeficient 3/2, ki se je pojavil v njem, je povezan s številom stopenj svobode v enem atomu. Ima sposobnost premikanja samo v eni od treh smeri prostora, to pomeni, da obstajajo samo translacijske stopnje svobode.
Če sistem tvorijo dvoatomske molekule, se trem translacijskim stopnjam dodata še dve rotacijski stopnji. Zato izraz za CV postane:
CV=5/2R.
Potem bo vrednost γ:
γ=7/5=1, 4.
Upoštevajte, da ima dvoatomska molekula dejansko še eno vibracijsko stopnjo svobode, vendar se pri temperaturah nekaj sto Kelvinov ne aktivira in ne prispeva k toplotni kapaciteti.
Če so molekule plina sestavljene iz več kot dveh atomov, bodo imele 6 stopinj svobode. Adiabatski eksponent bo v tem primeru enak:
γ=4/3 ≈ 1, 33.
TorejTorej, ko se število atomov v molekuli plina poveča, se vrednost γ zmanjša. Če zgradite adiabatni graf v osi P-V, boste opazili, da se bo krivulja za enoatomski plin obnašala bolj ostro kot za poliatomski plin.
Adiabatni eksponent za mešanico plinov
Zgoraj smo pokazali, da vrednost γ ni odvisna od kemične sestave plinskega sistema. Vendar pa je odvisno od števila atomov, ki sestavljajo njegove molekule. Predpostavimo, da je sistem sestavljen iz N komponent. Atomski delež komponente i v zmesi je ai. Nato lahko za določitev adiabatskega eksponenta zmesi uporabite naslednji izraz:
γ=∑i=1N(aiγ i).
Kjer je γi vrednost γ za i-to komponento.
Ta izraz se lahko na primer uporabi za določitev γ zraka. Ker je sestavljen iz 99 % dvoatomskih molekul kisika in dušika, bi moral biti njegov adiabatski indeks zelo blizu vrednosti 1,4, kar potrjuje eksperimentalna določitev te vrednosti.






