Svet, v katerem živimo, je nepredstavljivo lep in poln številnih različnih procesov, ki določajo potek življenja. Vse te procese preučuje znana znanost - fizika. Ponuja priložnost, da dobimo vsaj nekaj idej o nastanku vesolja. V tem članku bomo obravnavali tak koncept, kot je molekularna kinetična teorija, njene enačbe, vrste in formule. Vendar, preden se premaknete na globlje preučevanje teh vprašanj, morate sami razjasniti sam pomen fizike in področja, ki jih preučuje.
Kaj je fizika?

Pravzaprav je to zelo obsežna znanost in morda ena najbolj temeljnih v zgodovini človeštva. Na primer, če je ista računalništvo povezana s skoraj vsemi področji človeške dejavnosti, pa naj gre za računalniško oblikovanje ali ustvarjanje risank, potem je fizika življenje samo, opis njegovih zapletenih procesov in tokov. Poskusimo razbrati njegov pomen in čim bolj poenostaviti razumevanje.
TorejTako je fizika znanost, ki se ukvarja s preučevanjem energije in snovi, povezav med njima, razlago številnih procesov, ki se dogajajo v našem velikem vesolju. Molekularno-kinetična teorija strukture snovi je le majhna kapljica v morju teorij in vej fizike.
Energija, ki jo ta znanost podrobno preučuje, je lahko predstavljena v različnih oblikah. Na primer v obliki svetlobe, gibanja, gravitacije, sevanja, elektrike in mnogih drugih oblik. V tem članku se bomo dotaknili molekularno kinetične teorije strukture teh oblik.
Študija materije nam daje predstavo o atomski strukturi snovi. Mimogrede, izhaja iz molekularno-kinetične teorije. Znanost o zgradbi snovi nam omogoča, da razumemo in najdemo smisel našega obstoja, razloge za nastanek življenja in samo vesolje. Poskusimo še preučiti molekularno kinetično teorijo snovi.
Najprej je potreben nekaj uvoda za popolno razumevanje terminologije in morebitnih zaključkov.
teme iz fizike
Ko odgovarjamo na vprašanje, kaj je molekularno-kinetična teorija, ne moremo le govoriti o odsekih fizike. Vsak od teh se ukvarja s podrobno študijo in razlago določenega področja človeškega življenja. Razvrščeni so na naslednji način:
- Mehanika, ki je razdeljena na še dva dela: kinematika in dinamika.
- Statično.
- Termodinamika.
- Molekularni odsek.
- Elektrodinamika.
- Optics.
- Fizika kvantov in atomskega jedra.
Pogovorimo se posebej o molekularnifizike, ker temelji na molekularno-kinetični teoriji.
Kaj je termodinamika?
Na splošno sta molekularni del in termodinamika tesno povezani veji fizike, ki proučujeta izključno makroskopsko komponento celotnega števila fizikalnih sistemov. Ne smemo pozabiti, da te znanosti natančno opisujejo notranje stanje teles in snovi. Na primer njihovo stanje med segrevanjem, kristalizacijo, uparjanjem in kondenzacijo na atomski ravni. Z drugimi besedami, molekularna fizika je znanost o sistemih, ki so sestavljeni iz ogromnega števila delcev: atomov in molekul.
Te znanosti so preučevale glavne določbe molekularne kinetične teorije.
Že v sedmem razredu smo se seznanili s pojmi mikro- in makro-svetov, sistemov. Ne bo odveč, če osvežite te izraze v spominu.
Mikrosvet, kot lahko razberemo že iz njegovega imena, je sestavljen iz elementarnih delcev. Z drugimi besedami, to je svet majhnih delcev. Njihove velikosti se merijo v razponu od 10-18 m do 10-4 m, čas njihovega dejanskega stanja pa lahko doseže neskončnost in nesorazmerno majhni intervali, na primer 10-20 s.
Makrosvet obravnava telesa in sisteme stabilnih oblik, sestavljenih iz številnih elementarnih delcev. Takšni sistemi so sorazmerni z našo človeško velikostjo.
Poleg tega obstaja nekaj, kot je mega svet. Sestavljen je iz ogromnih planetov, kozmičnih galaksij in kompleksov.
Osnoveteorija
Zdaj, ko smo malo povzeli in se spomnili osnovnih izrazov fizike, lahko gremo neposredno na glavno temo tega članka.
Molekularno-kinetična teorija se je pojavila in je bila prvič oblikovana v devetnajstem stoletju. Njegovo bistvo je v tem, da podrobno opisuje strukturo katere koli snovi (pogosteje strukturo plinov kot trdnih in tekočih teles), ki temelji na treh temeljnih določbah, ki so bile zbrane iz domnev tako uglednih znanstvenikov, kot so Robert Hooke, Isaac. Newton, Daniel Bernoulli, Mikhail Lomonosov in mnogi drugi.
Glavne določbe molekularne kinetične teorije zvenijo takole:
- Absolutno vse snovi (ne glede na to, ali so tekoče, trdne ali plinaste) imajo kompleksno strukturo, sestavljeno iz manjših delcev: molekul in atomov. Atome včasih imenujemo "elementarne molekule".
- Vsi ti osnovni delci so vedno v stanju neprekinjenega in kaotičnega gibanja. Vsak od nas je naletel na neposreden dokaz te trditve, vendar mu najverjetneje ni pripisoval velikega pomena. Vsi smo na primer v ozadju sončnih žarkov videli, da se prašni delci nenehno premikajo v kaotični smeri. To je posledica dejstva, da atomi med seboj ustvarjajo medsebojne potiske in si med seboj nenehno prenašajo kinetično energijo. Ta pojav so prvič preučevali leta 1827 in so ga poimenovali po odkritelju - "Brownovo gibanje".
- Vsi elementarni delci so v procesu neprekinjene interakcije med sebojdoločene sile, ki imajo električni kamen.
Omeniti velja, da je še en primer, ki opisuje položaj številka dva, ki se lahko uporablja tudi na primer za molekularno kinetično teorijo plinov, difuzija. Z njim se srečujemo v vsakdanjem življenju ter pri številnih testih in kontrolah, zato je pomembno, da imamo o tem predstavo.
Najprej upoštevajte naslednje primere:
Zdravnik je pomotoma polil alkohol iz bučke na mizo. Ali pa ste morda spustili steklenico parfuma in se je razširila po tleh.
Zakaj bosta v teh dveh primerih tako vonj po alkoholu kot vonj po parfumu čez nekaj časa napolnila celotno sobo in ne samo predela, kjer se je vsebina teh snovi razlila?
Odgovor je preprost: difuzija.
Difuzija - kaj je to? Kako teče?

To je proces, pri katerem delci, ki sestavljajo eno določeno snov (običajno plin), prodrejo v medmolekularne praznine druge. V naših zgornjih primerih se je zgodilo naslednje: zaradi toplotnega, torej neprekinjenega in disociiranega gibanja, so molekule alkohola in/ali parfuma padle v reže med molekulami zraka. Postopoma se pod vplivom trka z atomi in molekulami zraka širijo po prostoru. Mimogrede, intenzivnost difuzije, to je hitrost njenega toka, je odvisna od gostote snovi, ki sodelujejo pri difuziji, pa tudi od energije gibanja njihovih atomov in molekul, ki se imenuje kinetična. Večja kot je kinetična energija, večja je hitrost teh molekul in intenzivnost.
Najhitrejši proces difuzije lahko imenujemo difuzija v plinih. To je posledica dejstva, da plin po svoji sestavi ni homogen, kar pomeni, da medmolekularne praznine v plinih zasedajo veliko prostora oziroma proces pridobivanja atomov in molekul tuje snovi vanje poteka lažje in hitreje..
Ta postopek je v tekočinah nekoliko počasnejši. Raztapljanje sladkornih kock v skodelici čaja je le primer difuzije trdne snovi v tekočini.
Toda najdaljši čas je difuzija v telesih s trdno kristalno strukturo. Točno tako, saj je struktura trdnih snovi homogena in ima močno kristalno mrežo, v celicah katere vibrirajo atomi trdne snovi. Če na primer površine dveh kovinskih palic dobro očistimo in nato pripeljemo v stik med seboj, potem bomo po dovolj dolgem času lahko zaznali koščke ene kovine v drugi in obratno.
Kot kateri koli drugi temeljni odsek je tudi osnovna fizikalna teorija razdeljena na ločene dele: klasifikacijo, vrste, formule, enačbe itd. Tako smo se naučili osnov molekularne kinetične teorije. To pomeni, da lahko varno nadaljujete z obravnavo posameznih teoretičnih blokov.
Molekularno-kinetična teorija plinov
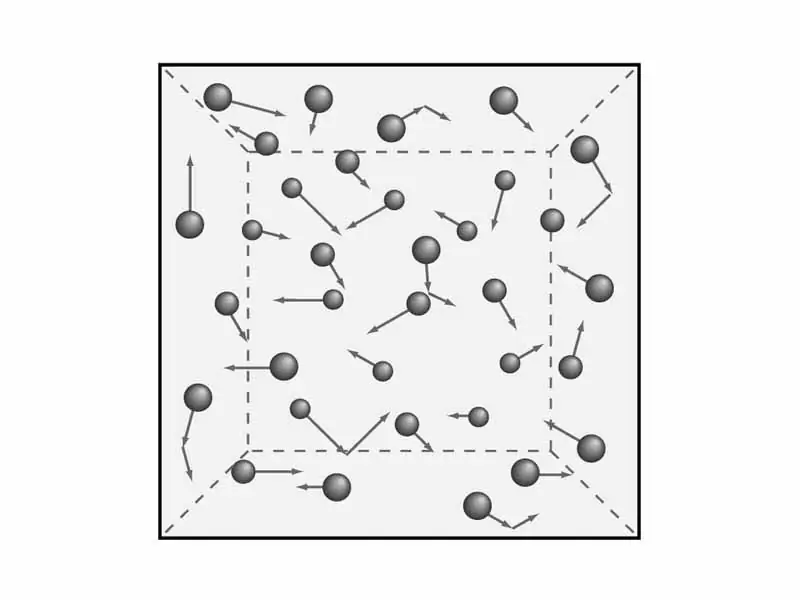
Obstaja potreba po razumevanju določil teorije plina. Kot smo že povedali, bomo upoštevali makroskopske značilnosti plinov, kot sta tlak in temperatura. To jebo potreben kasneje za izpeljavo enačbe molekularno-kinetične teorije plinov. Toda matematika - kasneje, zdaj pa se ukvarjajmo s teorijo in s tem s fiziko.
Znanstveniki so oblikovali pet določb molekularne teorije plinov, ki služijo za razumevanje kinetičnega modela plinov. Zvenijo takole:
- Vsi plini so sestavljeni iz elementarnih delcev, ki nimajo določene velikosti, imajo pa določeno maso. Z drugimi besedami, prostornina teh delcev je minimalna v primerjavi z dolžino med njimi.
- Atomi in molekule plinov praktično nimajo potencialne energije, oziroma je po zakonu vsa energija enaka kinetični.
- S tem položajem smo se že seznanili prej - Brownovo gibanje. To pomeni, da so delci plina vedno v neprekinjenem in kaotičnem gibanju.
- Absolutno vsi medsebojni trki plinskih delcev, ki jih spremlja sporočilo hitrosti in energije, so popolnoma elastični. To pomeni, da med trkom ni izgube energije ali ostrih skokov njihove kinetične energije.
- Pod normalnimi pogoji in konstantno temperaturo je povprečna energija gibanja delcev skoraj vseh plinov enaka.
Peti položaj lahko prepišemo s to vrsto enačbe molekularno-kinetične teorije plinov:
E=1/2mv^2=3/2kT, kjer je k Boltzmannova konstanta; T - temperatura v Kelvinih.
Ta enačba nam pomaga razumeti razmerje med hitrostjo osnovnih delcev plina in njihovo absolutno temperaturo. V skladu s tem višji je njihov absoluttemperatura, večja je njihova hitrost in kinetična energija.
tlak plina
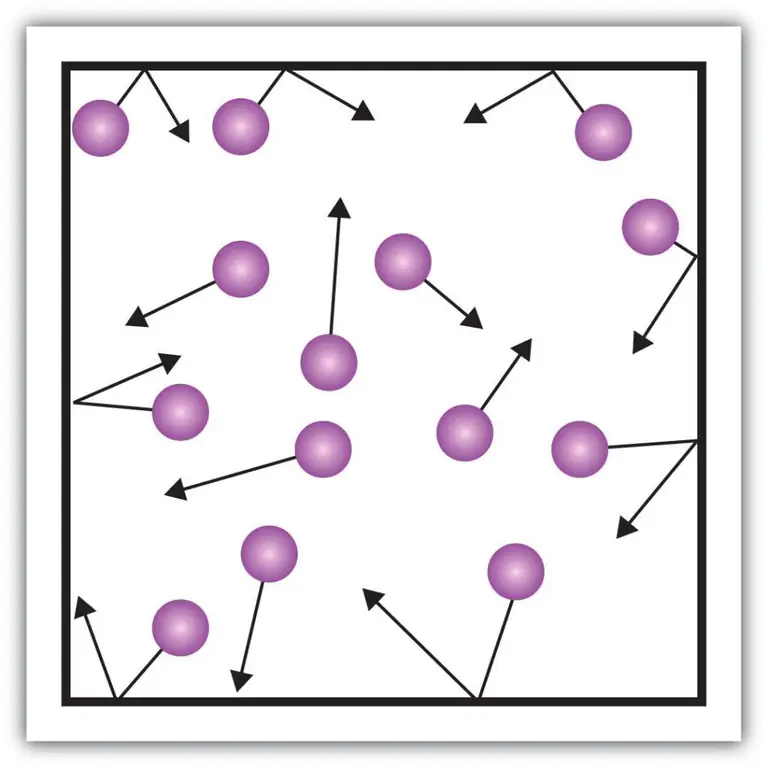
Takšne makroskopske komponente lastnosti, kot je tlak plinov, je mogoče razložiti tudi s pomočjo kinetične teorije. Če želite to narediti, si predstavljajmo naslednji primer.
Predpostavimo, da je molekula nekega plina v škatli, katere dolžina je L. Uporabimo določbe zgoraj opisane teorije plinov in upoštevajmo dejstvo, da se molekularna krogla giblje le vzdolž x -os. Tako bomo lahko opazovali proces elastičnega trka z eno od sten posode (škatle).
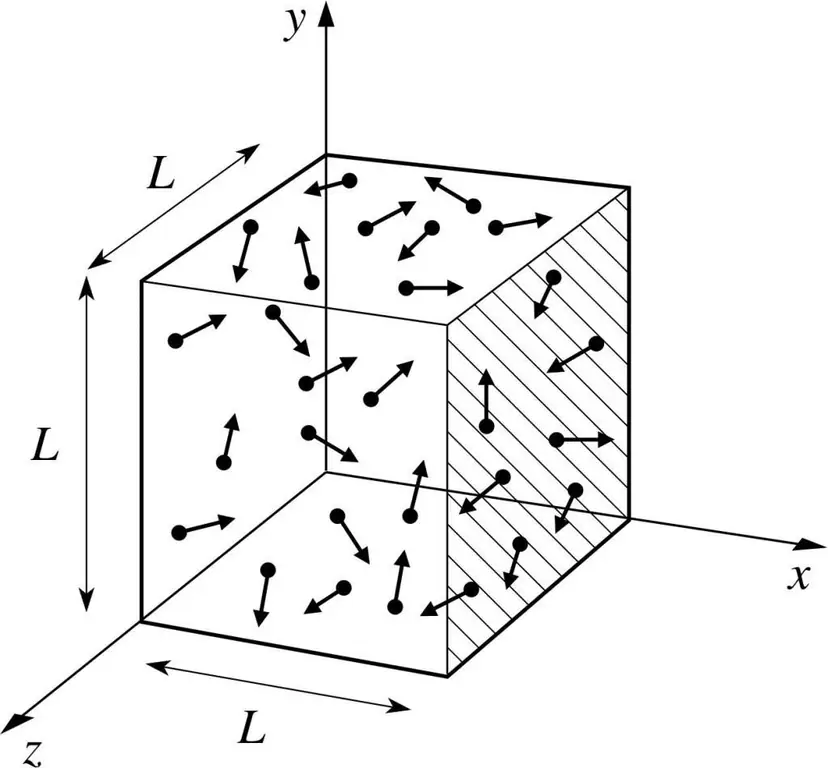
Zagon trenutnega trka, kot vemo, je določen s formulo: p=mv, vendar bo v tem primeru ta formula dobila obliko projekcije: p=mv(x).
Ker upoštevamo samo dimenzijo osi x, to je os x, bo skupna sprememba zagona izražena s formulo: mv(x) - m(-v(x))=2mv(x).
Naprej razmislite o sili, ki jo izvaja naš predmet z uporabo Newtonovega drugega zakona: F=ma=P/t.
Iz teh formul izrazimo tlak s strani plina: P=F/a;
Zdaj zamenjajmo izraz sile v dobljeno formulo in dobimo: P=mv(x)^2/L^3.
Po tem lahko našo končno formulo tlaka zapišemo za N-to število molekul plina. Z drugimi besedami, izgledalo bo takole:
P=Nmv(x)^2/V, kjer je v hitrost in V glasnost.
Sedaj poskusimo izpostaviti nekaj osnovnih določb o tlaku plina:
- Manifestira se skozitrki molekul z molekulami sten predmeta, v katerem se nahaja.
- Velikost tlaka je premosorazmerna s silo in hitrostjo udarca molekul na stene posode.
Nekaj kratkih zaključkov o teoriji
Preden gremo dlje in razmislimo o osnovni enačbi molekularne kinetične teorije, vam ponujamo nekaj kratkih zaključkov iz zgornjih točk in teorije:
- Merilo povprečne energije gibanja njegovih atomov in molekul je absolutna temperatura.
- Ko sta dva različna plina pri isti temperaturi, imata njune molekule enako povprečno kinetično energijo.
- Energija plinskih delcev je neposredno sorazmerna s srednjo kvadratno hitrostjo: E=1/2mv^2.
- Čeprav imajo molekule plina povprečno kinetično energijo oziroma povprečno hitrost, se posamezni delci premikajo z različnimi hitrostmi: nekateri hitro, drugi počasi.
- Višja kot je temperatura, višja je hitrost molekul.
- Kolikokrat povečamo temperaturo plina (na primer dvakrat), se energija gibanja njegovih delcev tolikokrat poveča (oziroma podvoji).
Osnovna enačba in formule

Osnovna enačba molekularne kinetične teorije vam omogoča, da vzpostavite razmerje med količinami mikrosveta in s tem makroskopskimi, torej merjenimi količinami.
Eden najpreprostejših modelov, ki jih molekularna teorija lahko upošteva, je model idealnega plina.
Lahko bi tako reklito je neke vrste imaginarni model, ki ga preučuje molekularno kinetična teorija idealnega plina, v katerem:
- najpreprostejši delci plina veljajo za popolnoma elastične kroglice, ki medsebojno delujejo med seboj in z molekulami sten katere koli posode samo v enem primeru - absolutno elastičen trk;
- privlačne sile v plinu so odsotne ali pa jih je dejansko mogoče zanemariti;
- elemente notranje strukture plina lahko vzamemo kot materialne točke, torej lahko zanemarimo tudi njihov volumen.
Ob upoštevanju takšnega modela je nemški fizik Rudolf Clausius napisal formulo za tlak plina prek razmerja mikro- in makroskopskih parametrov. Izgleda tako:
p=1/3m(0)nv^2.
Pozneje bo ta formula imenovana kot osnovna enačba molekularno-kinetične teorije idealnega plina. Lahko se predstavi v več različnih oblikah. Naša dolžnost je zdaj pokazati odseke, kot so molekularna fizika, molekularna kinetična teorija in s tem njihove popolne enačbe in vrste. Zato je smiselno razmisliti o drugih različicah osnovne formule.
Vemo, da lahko povprečno energijo, ki označuje gibanje plinskih molekul, najdemo s formulo: E=m(0)v^2/2.
V tem primeru lahko zamenjamo izraz m(0)v^2 v izvirni formuli tlaka s povprečno kinetično energijo. Kot rezultat tega bomo imeli možnost sestaviti osnovno enačbo molekularno-kinetične teorije plinov v naslednji obliki: p=2/3nE.
Poleg tega vsi vemo, da lahko izraz m(0)n zapišemo kot produkt dveh količnikov:
m/NN/V=m/V=ρ.
Po teh manipulacijah lahko prepišemo našo formulo za enačbo molekularno-kinetične teorije idealnega plina v tretji, drugačni obliki:
p=1/3ρv^2.
No, morda je to vse, kar morate vedeti o tej temi. Ostaja samo sistematizirati pridobljeno znanje v obliki kratkih (in ne tako) zaključkov.
Vsi splošni zaključki in formule na temo "Molekularno-kinetična teorija"
Torej začnimo.
prvi:
Fizika je temeljna veda, vključena v naravoslovje, ki preučuje lastnosti snovi in energije, njihovo strukturo, vzorce anorganske narave.
Vključuje naslednje razdelke:
- mehanika (kinematika in dinamika);
- statična;
- termodinamika;
- elektrodinamika;
- molekularni odsek;
- optika;
- fizika kvantov in atomskega jedra.
drugi:
Fizika delcev in termodinamika sta tesno povezani veji, ki proučujeta izključno makroskopsko komponento celotnega števila fizičnih sistemov, torej sistemov, sestavljenih iz ogromnega števila elementarnih delcev.
Temeljijo na molekularno kinetični teoriji.
tretji:
Bistvo zadeve je to. Molekularna kinetična teorija podrobno opisuje strukturo snovi (pogosteje strukturo plinov kot trdnih snovi).in tekočih teles), ki temelji na treh temeljnih predpostavkah, ki so bile zbrane iz domnev uglednih znanstvenikov. Med njimi: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov in mnogi drugi.
četrti:
Tri osnovna načela molekularne kinetične teorije:
- Vse snovi (ne glede na to, ali so tekoče, trdne ali plinaste) imajo kompleksno strukturo, sestavljeno iz manjših delcev: molekul in atomov.
- Vsi ti preprosti delci so v neprekinjenem kaotičnem gibanju. Primer: Brownovo gibanje in difuzija.
- Vse molekule pod kakršnimi koli pogoji medsebojno delujejo z določenimi silami, ki imajo električni kamen.
Vsaka od teh določil molekularne kinetične teorije je trdna podlaga pri preučevanju strukture snovi.
Peti:
Več glavnih točk molekularne teorije za plinski model:
- Vsi plini so sestavljeni iz elementarnih delcev, ki nimajo določene velikosti, imajo pa določeno maso. Z drugimi besedami, prostornina teh delcev je minimalna v primerjavi z razdaljami med njimi.
- Atomi in molekule plinov praktično nimajo potencialne energije, njihova skupna energija je enaka kinetični.
- S tem položajem smo se že seznanili prej - Brownovo gibanje. To pomeni, da so delci plina vedno v neprekinjenem in naključnem gibanju.
- Absolutno vsi medsebojni trki atomov in molekul plinov, ki jih spremlja sporočilo hitrosti in energije, so popolnoma elastični. To jepomeni, da med trkom ni izgube energije ali ostrih skokov njihove kinetične energije.
- Pod normalnimi pogoji in konstantno temperaturo je povprečna kinetična energija skoraj vseh plinov enaka.
šesto:
Sklepi iz teorije o plinih:
- Absolutna temperatura je merilo povprečne kinetične energije njenih atomov in molekul.
- Ko sta dva različna plina pri isti temperaturi, imata njune molekule enako povprečno kinetično energijo.
- Povprečna kinetična energija plinskih delcev je neposredno sorazmerna s povprečno kvadratno hitrostjo: E=1/2mv^2.
- Čeprav imajo molekule plina povprečno kinetično energijo oziroma povprečno hitrost, se posamezni delci premikajo z različnimi hitrostmi: nekateri hitro, drugi počasi.
- Višja kot je temperatura, višja je hitrost molekul.
- Kolikokrat povečamo temperaturo plina (na primer dvakrat), se tolikokrat poveča tudi povprečna kinetična energija njegovih delcev (oziroma podvoji).
- Razmerje med tlakom plina na stene posode, v kateri se nahaja, in intenzivnostjo udarcev molekul na te stene je premo sorazmerno: več udarcev, višji je tlak in obratno.
Sedmi:
Model idealnega plina je model, v katerem morajo biti izpolnjeni naslednji pogoji:
- Plinske molekule lahko in veljajo za popolnoma elastične kroglice.
- Te kroglice lahko delujejo med seboj in s stenami katere koliplovilo samo v enem primeru - popolnoma elastičen trk.
- Tiste sile, ki opisujejo medsebojni potisk med atomi in molekulami plina, so odsotne ali pa jih je mogoče dejansko zanemariti.
- Atomi in molekule se obravnavajo kot materialne točke, to pomeni, da je njihov volumen mogoče zanemariti.
Osma:
Podajmo vse osnovne enačbe in pokažimo formule v temi "Molekularno-kinetična teorija":
p=1/3m(0)nv^2 - osnovna enačba za model idealnega plina, ki jo je izpeljal nemški fizik Rudolf Clausius.
p=2/3nE - osnovna enačba molekularno-kinetične teorije idealnega plina. Izhaja iz povprečne kinetične energije molekul.
р=1/3ρv^2 - ista enačba, vendar upoštevana preko gostote in srednje kvadratne hitrosti molekul idealnega plina.
m(0)=M/N(a) - formula za iskanje mase ene molekule preko Avogadrovega števila.
v^2=(v(1)+v(2)+v(3)+…)/N - formula za iskanje srednje kvadratne hitrosti molekul, kjer je v(1), v(2), v (3) in tako naprej - hitrost prve molekule, druge, tretje in tako naprej do n-te molekule.
n=N/V - formula za iskanje koncentracije molekul, kjer je N število molekul v prostornini plina na dano prostornino V.
E=mv^2/2=3/2kT - formule za iskanje povprečne kinetične energije molekul, kjer je v^2 povprečna kvadratna hitrost molekul, k je konstanta vrednost poimenovana po avstrijski fiziki Ludwiga Boltzmanna, T pa je temperatura plina.
p=nkT - formula za tlak v smislu koncentracije, konstantnaBoltzmanna in absolutne temperature T. Iz nje sledi še ena temeljna formula, ki sta jo odkrila ruski znanstvenik Mendelejev in francoski fizik-inženir Claiperon:
pV=m/MRT, kjer je R=kN(a) univerzalna konstanta za pline.
Zdaj pokažimo konstante za različne izoprocese: izobarične, izohorične, izotermne in adiabatske.
pV/T=const - izvede se, ko sta masa in sestava plina konstantni.
рV=const - če je tudi temperatura konstantna.
V/T=const - če je tlak plina konstanten.
p/T=const - če je glasnost konstantna.
Morda je to vse, kar morate vedeti o tej temi.
Danes smo se potopili v tako znanstveno področje, kot je teoretična fizika, njeni številni odseki in bloki. Podrobneje smo se dotaknili takšnega področja fizike, kot sta temeljna molekularna fizika in termodinamika, in sicer molekularno-kinetična teorija, ki v začetni študiji, kot se zdi, ne predstavlja težav, v resnici pa ima veliko pasti.. Razširja naše razumevanje modela idealnega plina, ki smo ga tudi podrobno preučili. Poleg tega velja omeniti, da smo se seznanili tudi z osnovnimi enačbami molekularne teorije v njihovih različnih variacijah, upoštevali pa smo tudi vse najnujnejše formule za iskanje določenih neznanih količin na to temo. To bo še posebej koristno pri pripravi pisanja kakršne koli teste, izpite in teste ali za razširitev splošnega pogleda in znanja o fiziki.
Upamo, da vam je bil ta članek koristen in ste iz njega izluščili le najnujnejše informacije, s čimer ste okrepili svoje znanje o takšnih stebrih termodinamike, kot so osnovne določbe molekularne kinetične teorije.






